23/06/2010
El amoniaco, ese gas de olor penetrante y característico que muchos asocian con productos de limpieza, es mucho más que eso. Se trata de un compuesto químico fundamental, el trihidruro de nitrógeno (NH3), cuya producción a gran escala es pilar de numerosas industrias a nivel global. Su versatilidad lo convierte en un ingrediente esencial en áreas tan diversas como la agricultura, la fabricación de productos farmacéuticos y la producción de plásticos.

Aunque el amoniaco se genera de manera natural a través de la descomposición de materia orgánica, la demanda mundial supera con creces lo que la naturaleza puede ofrecer. Esto ha impulsado el desarrollo de procesos industriales sofisticados para su síntesis, siendo el más relevante y extendido a lo largo de la historia el aclamado proceso de Haber-Bosch. Entender cómo se obtiene industrialmente este compuesto es clave para comprender su impacto en nuestra sociedad y economía.
- ¿Qué es Exactamente el Amoniaco (NH3)?
- El Proceso de Haber-Bosch: La Síntesis del Amoniaco a Gran Escala
- Materias Primas Clave para la Síntesis de Amoniaco
- Una Mirada a la Evolución de la Producción Industrial
- Tecnologías Modernas en la Síntesis de Amoniaco
- Amoniaco Gris vs. Amoniaco Verde: El Futuro Sostenible
- Producción de Amoniaco a partir de Carbón
- Principales Usos del Amoniaco
- Seguridad y Control en Plantas de Amoniaco
- Preguntas Frecuentes sobre el Amoniaco
- Conclusión
¿Qué es Exactamente el Amoniaco (NH3)?
El amoniaco (NH3) es un compuesto químico formado por un átomo de nitrógeno y tres átomos de hidrógeno. En condiciones normales de presión y temperatura, se presenta como un gas incoloro con un olor fuertemente desagradable y picante. Es fácilmente soluble en agua, formando hidróxido de amonio (NH4OH), que es la forma líquida en la que a menudo se comercializa para usos domésticos e industriales.
Es importante destacar que, aunque útil, el amoniaco es una sustancia cáustica y potencialmente peligrosa si no se maneja adecuadamente. Su naturaleza lo hace reactivo y valioso en diversas aplicaciones químicas.
El Proceso de Haber-Bosch: La Síntesis del Amoniaco a Gran Escala
La piedra angular de la producción industrial de amoniaco es el proceso de Haber-Bosch, nombrado así en honor a sus desarrolladores, los químicos alemanes Fritz Haber y Carl Bosch. Este ingenioso método, desarrollado a principios del siglo XX, permitió por primera vez la síntesis de amoniaco a partir de elementos abundantes y accesibles: nitrógeno del aire e hidrógeno, inicialmente obtenido de diversas fuentes, pero hoy predominantemente del gas natural.
La reacción química fundamental es la siguiente:
N₂(g) + 3H₂(g) → 2NH₃(g)
Esta reacción, aparentemente simple, presenta desafíos significativos. El nitrógeno molecular (N₂) es una molécula muy estable debido a su triple enlace, lo que requiere una gran cantidad de energía de activación para romperlo y permitir que reaccione con el hidrógeno. En condiciones normales, la reacción es extremadamente lenta y el equilibrio favorece la formación de los reactivos (nitrógeno e hidrógeno) en lugar del producto (amoniaco).
Para superar estas limitaciones y hacer que el proceso sea económicamente viable a escala industrial, se emplean condiciones de operación específicas:
- Altas Presiones: Típicamente entre 150 y 350 bares (aunque históricamente se usaron presiones mucho mayores). Según el principio de Le Chatelier, aumentar la presión favorece la formación de amoniaco, ya que la reacción implica una disminución del número total de moles gaseosos (4 moles de reactivos se convierten en 2 moles de producto).
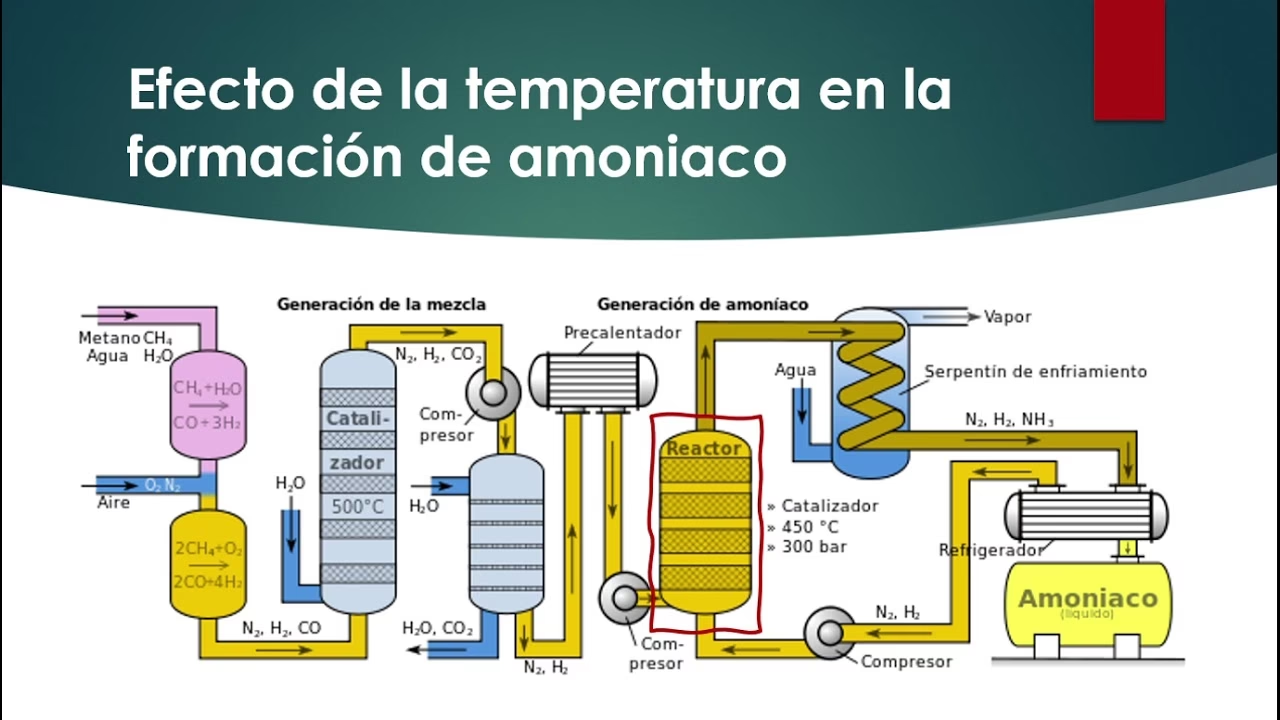
- Temperaturas Moderadamente Altas: Generalmente entre 400°C y 500°C. Si bien una temperatura más baja favorecería el equilibrio hacia la formación de amoniaco (la reacción es exotérmica), una temperatura suficientemente alta es necesaria para que la velocidad de reacción sea práctica.
- Uso de un Catalizador: Este es un componente crucial. Se utiliza un catalizador de base de hierro (promovido con óxidos de potasio, calcio, aluminio y otros) para acelerar significativamente la velocidad de la reacción, permitiendo que se alcance el equilibrio en un tiempo razonable a las temperaturas y presiones de operación.
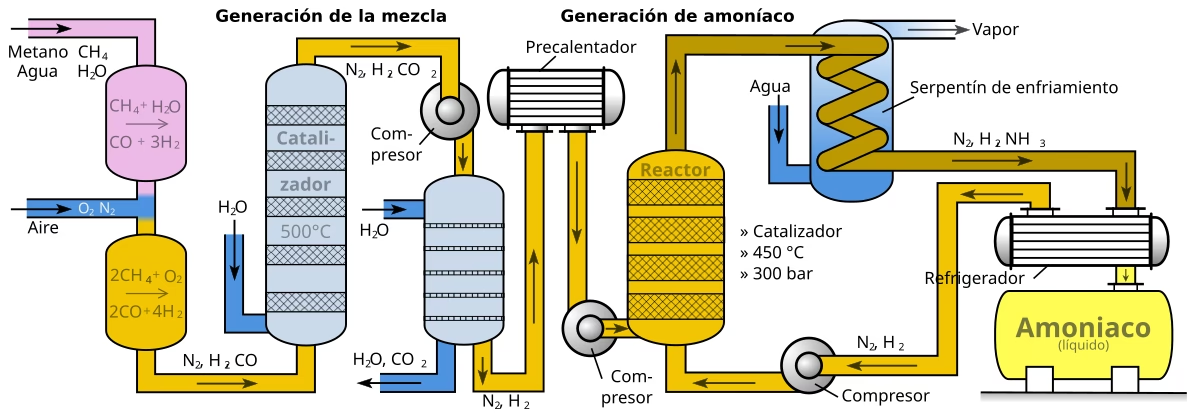
El proceso implica la mezcla de nitrógeno e hidrógeno en la proporción estequiométrica 1:3, su compresión a alta presión y su paso a través de un reactor (convertidor) que contiene el lecho catalítico y opera a alta temperatura. La reacción produce amoniaco, pero la conversión por paso es incompleta (típicamente 15-25%). Por lo tanto, la mezcla de gases de salida se enfría para condensar el amoniaco (que se separa como líquido) y los gases no reaccionados (nitrógeno e hidrógeno), junto con pequeñas cantidades de inertes (como argón y metano), se recirculan al reactor después de añadir gas fresco.
Materias Primas Clave para la Síntesis de Amoniaco
La producción de amoniaco, especialmente a través del proceso Haber-Bosch, depende fundamentalmente de dos reactivos: nitrógeno e hidrógeno.
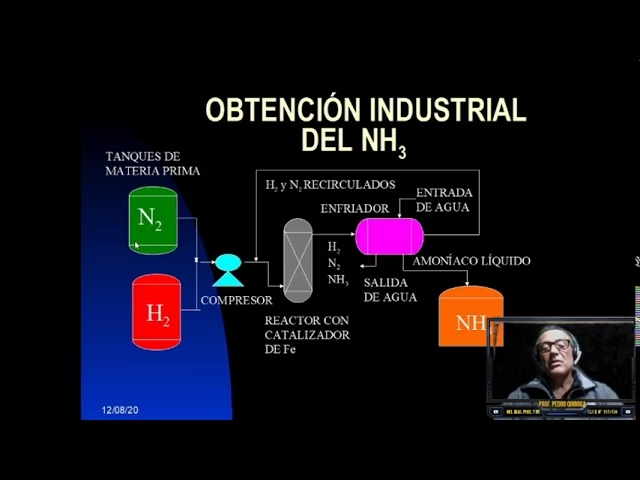
- Nitrógeno (N₂): La fuente de nitrógeno es sencilla: se obtiene directamente del aire atmosférico. El aire está compuesto aproximadamente en un 78% por nitrógeno. Este se separa del oxígeno y otros componentes del aire mediante procesos de separación criogénica (licuefacción y destilación del aire) o, en algunos casos, mediante adsorción por cambio de presión (PSA).
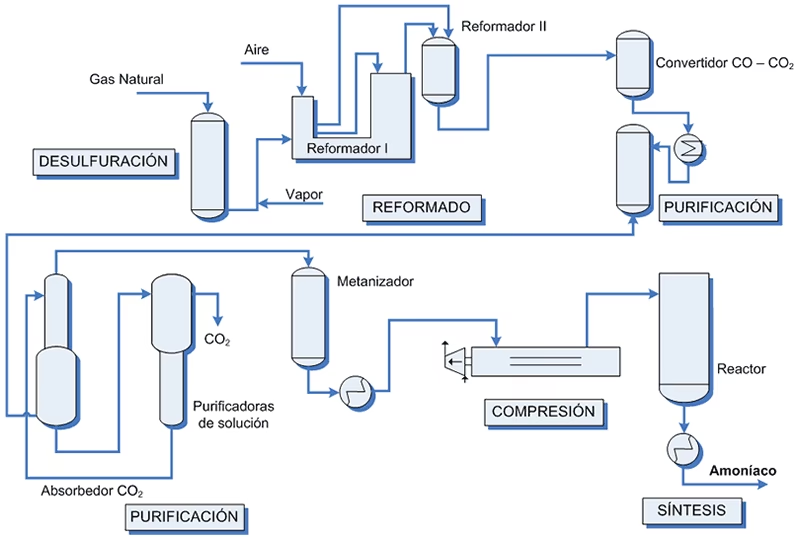
- Hidrógeno (H₂): La obtención del hidrógeno es el paso más complejo y energéticamente intensivo del proceso y, a menudo, determina el costo y el impacto ambiental de la producción de amoniaco. Históricamente, el hidrógeno se obtenía de la gasificación del carbón o la electrólisis del agua. Sin embargo, la gran mayoría del hidrógeno para la producción de amoniaco "gris" actual proviene del reformado con vapor de gas natural (principalmente metano, CH₄). Este proceso implica hacer reaccionar el gas natural con vapor de agua a altas temperaturas para producir hidrógeno y monóxido de carbono (CO). Posteriormente, el CO se convierte en más hidrógeno y dióxido de carbono (CO₂) mediante la reacción de desplazamiento de gas de agua (water-gas shift reaction). El CO₂ se elimina antes de la síntesis de amoniaco. Otras fuentes de hidrógeno incluyen la gasificación de otros hidrocarburos (como nafta) o la gasificación del carbón, procesos aún importantes en regiones con abundantes reservas de carbón, como China.
La eficiencia y el impacto ambiental de una planta de amoniaco están estrechamente ligados a cómo se obtiene el hidrógeno.
Una Mirada a la Evolución de la Producción Industrial
Desde el primer aislamiento del amoniaco por Joseph Priestley en 1774 hasta la puesta en marcha de la primera planta comercial de Haber-Bosch por BASF en Oppau, Alemania, en 1913, la producción de amoniaco ha experimentado una notable evolución. Las primeras plantas eran relativamente pequeñas y operaban a presiones muy altas utilizando compresores reciprocantes y diseños multi-tren.
La verdadera revolución llegó a mediados del siglo XX con el desarrollo de las plantas de amoniaco de una sola línea (single-train). Innovaciones como el uso de compresores centrífugos de gran capacidad, la optimización masiva de la recuperación de calor residual para generar vapor que impulsaba las turbinas de los compresores, y un diseño de planta altamente integrado permitieron construir instalaciones mucho más grandes, eficientes y con menores costos operativos. La capacidad de una sola línea pasó de unos pocos cientos de toneladas por día a superar las 3000 toneladas por día en las plantas modernas.
La reducción de la presión de operación en el lazo de síntesis (de más de 300 bares a 150-200 bares) fue otra mejora significativa. Aunque requirió más catalizador, permitió el uso de equipos más ligeros y menos costosos, facilitando la implementación de las plantas de gran escala.
Tecnologías Modernas en la Síntesis de Amoniaco
El campo de la producción de amoniaco sigue evolucionando, con constantes mejoras en la eficiencia energética, la capacidad de producción y la integración de procesos. Los principales licenciadores de tecnología, como KBR, Haldor Topsøe, ThyssenKrupp Industrial Solutions (TKIS), Linde (LAC) y Ammonia Casale, ofrecen diversas variantes del proceso básico de Haber-Bosch, incorporando innovaciones específicas:
- Diseños Optimizados del Front-End: Mejora en el reformado (primario y secundario), sistemas de purificación de gas de síntesis (como lavados de nitrógeno criogénico o PSA) para eliminar inertes y ajustar la relación H₂/N₂.
- Convertidores de Síntesis Avanzados: Desarrollo de convertidores con lechos catalíticos de flujo radial o axial-radial, que ofrecen menor caída de presión y mayor eficiencia de conversión por paso. Algunos diseños incorporan intercambiadores de calor internos.
- Catalizadores Mejorados: Desarrollo de catalizadores más activos y resistentes, incluyendo catalizadores de hierro promovido y, en algunos casos, catalizadores a base de rutenio para condiciones específicas.
- Máxima Recuperación de Energía: Sistemas de recuperación de calor residual altamente eficientes que generan vapor de alta presión para turbinas, optimizando el balance energético de la planta.
- Lazos de Síntesis de Baja Energía: Diseños que minimizan el consumo energético de los compresores y maximizan la conversión.
La competencia en el mercado impulsa la búsqueda continua de soluciones que reduzcan el consumo de energía (actualmente por debajo de 28 GJ/tonelada de amoniaco en las mejores plantas modernas) y los costos de producción.
Amoniaco Gris vs. Amoniaco Verde: El Futuro Sostenible
La producción convencional de amoniaco, el llamado amoniaco "gris", tiene una huella de carbono significativa. Como mencionamos, el hidrógeno se obtiene principalmente del reformado de gas natural, un proceso que libera grandes cantidades de dióxido de carbono (CO₂). Se estima que por cada tonelada de amoniaco gris producida, se emiten aproximadamente 2 toneladas de CO₂.
Ante la creciente preocupación por el cambio climático, ha surgido con fuerza el concepto de amoniaco "verde". El amoniaco verde se produce utilizando hidrógeno "verde", que se obtiene mediante la electrólisis del agua. La clave es que la energía eléctrica utilizada para la electrólisis proviene exclusivamente de fuentes de energía renovable (solar, eólica, hidráulica, etc.). De esta manera, todo el proceso, desde la generación de hidrógeno hasta la síntesis de amoniaco (que sigue siendo típicamente el proceso Haber-Bosch, pero alimentado con H₂ verde), se realiza con una emisión mínima o nula de CO₂.
Aunque actualmente el volumen de producción de amoniaco verde es pequeño en comparación con el amoniaco gris (que domina un mercado global de alrededor de 185 millones de toneladas anuales), se espera un crecimiento exponencial en las próximas décadas. El amoniaco verde no solo reemplazará gradualmente al gris en sus usos tradicionales, sino que también se vislumbra como un potencial combustible o portador de hidrógeno para el sector energético y de transporte, dada su facilidad de licuefacción y transporte en comparación con el hidrógeno puro.
| Característica | Amoniaco Gris | Amoniaco Verde |
|---|---|---|
| Fuente de Hidrógeno | Principalmente reformado de gas natural | Electrólisis del agua |
| Fuente de Energía | Principalmente combustibles fósiles | Fuentes de energía renovable |
| Emisiones de CO₂ | Altas (aprox. 2 ton CO₂/ton NH₃) | Muy bajas o nulas |
| Proceso de Síntesis | Haber-Bosch | Típicamente Haber-Bosch |
| Impacto Ambiental | Alta huella de carbono | Baja o nula huella de carbono |
| Costo Actual | Generalmente menor | Generalmente mayor (depende del costo de la energía renovable) |
| Volumen de Producción Global | Dominante (aprox. 99%) | Emergente (aprox. 1%) |
Producción de Amoniaco a partir de Carbón
En países con grandes reservas de carbón, como China, una parte significativa de la producción de amoniaco se basa en la gasificación del carbón. Este proceso es una alternativa al reformado de gas natural para obtener el gas de síntesis (mezcla de H₂ y CO) necesario para el proceso Haber-Bosch.
El proceso de producción de amoniaco a partir de carbón generalmente incluye las siguientes etapas:
- Unidad de Separación de Aire (ASU): Para obtener oxígeno (O₂) y nitrógeno (N₂) puros del aire.
- Gasificación del Carbón: El carbón reacciona con oxígeno y vapor a alta presión y temperatura en un gasificador para producir gas de síntesis (principalmente CO, H₂, CO₂ y CH₄).
- Conversión del Monóxido de Carbono (Water-Gas Shift): El CO se hace reaccionar con vapor para producir más H₂ y CO₂.
- Eliminación de Gases Ácidos (AGRU): Se eliminan el CO₂ y los compuestos de azufre del gas de síntesis.
- Purificación del Gas de Síntesis: Se eliminan los inertes y los componentes residuales (como metano y CO) mediante procesos como lavado con nitrógeno líquido o PSA para obtener una mezcla pura de H₂ y N₂ en la proporción correcta.
- Síntesis de Amoniaco: La mezcla purificada de H₂ y N₂ se alimenta al proceso Haber-Bosch.
Aunque este proceso permite aprovechar las reservas de carbón, suele ser menos eficiente energéticamente que el reformado de gas natural y genera mayores emisiones de CO₂ y otros contaminantes (si no se implementan tecnologías de captura y tratamiento adecuadas).
Principales Usos del Amoniaco
La inmensa mayoría del amoniaco producido a nivel mundial (aproximadamente el 88%) se destina a la fabricación de fertilizantes nitrogenados. Compuestos como la urea, el nitrato de amonio y el fosfato de amonio son esenciales para la agricultura moderna, permitiendo aumentar significativamente el rendimiento de los cultivos y, por ende, alimentar a una población mundial en crecimiento. Sin los fertilizantes basados en amoniaco, la producción de alimentos sería insuficiente para sostener a miles de millones de personas.
Además de su papel crucial en la agricultura, el amoniaco tiene una amplia variedad de otros usos industriales y domésticos:
- Productos de Limpieza: El amoniaco disuelto en agua es un potente desengrasante y quitamanchas, eficaz para limpiar diversas superficies, textiles e incluso para decapar muebles.
- Refrigeración: El amoniaco gaseoso es un refrigerante eficiente (R717) debido a su alta capacidad para absorber calor. Se utiliza en grandes instalaciones de refrigeración industrial (como almacenes frigoríficos) y sistemas de aire acondicionado, aunque requiere precauciones especiales debido a su toxicidad.
- Tratamiento de Aguas: Se emplea para ajustar el pH en calderas de vapor, minimizando la corrosión, y también en sistemas de tratamiento de aguas residuales.
- Industria Química: Es materia prima para la producción de una vasta gama de productos químicos, incluyendo explosivos, fibras sintéticas (como el nylon), plásticos, medicamentos, pesticidas y pinturas.
- Industria de la Celulosa y el Papel: Se utiliza en diversos procesos dentro de esta industria.
Seguridad y Control en Plantas de Amoniaco
Dada la naturaleza del amoniaco y las condiciones extremas de operación del proceso Haber-Bosch (alta presión, alta temperatura, gases inflamables y tóxicos), la seguridad es una prioridad máxima en las plantas de producción. Las instalaciones modernas incorporan sistemas de control distribuido (DCS) y sistemas instrumentados de seguridad (SIS) para monitorear y controlar rigurosamente todos los parámetros del proceso y garantizar una operación segura. Se realizan estudios detallados de riesgos (HAZOP) y análisis de capas de protección (LOPA) durante el diseño y la operación para identificar peligros y mitigar riesgos potenciales. La formación continua del personal es también fundamental para operar estas complejas instalaciones de manera segura y eficiente.
Preguntas Frecuentes sobre el Amoniaco
¿Es peligroso el amoniaco?
Sí, el amoniaco es cáustico y tóxico. En altas concentraciones, puede causar irritación severa en ojos, piel y vías respiratorias. El amoniaco gaseoso es inflamable en ciertas concentraciones en aire. Por ello, su manejo industrial requiere estrictas medidas de seguridad y equipos de protección.

¿Por qué es tan importante el proceso Haber-Bosch?
El proceso Haber-Bosch es considerado uno de los logros de ingeniería química más importantes del siglo XX. Permitió sintetizar amoniaco a gran escala de manera económica, haciendo posible la producción masiva de fertilizantes nitrogenados. Esto revolucionó la agricultura, permitiendo alimentar a una población mundial que creció exponencialmente, evitando hambrunas masivas.
¿Cuál es la diferencia principal entre amoniaco gris y verde?
La diferencia principal radica en la fuente de hidrógeno y, consecuentemente, en la huella de carbono. El amoniaco gris usa hidrógeno de combustibles fósiles (gas natural, carbón) emitiendo CO₂, mientras que el amoniaco verde usa hidrógeno producido por electrólisis alimentada con energía renovable, sin emisiones de CO₂.
¿Se puede usar amoniaco directamente como fertilizante?
Sí, el amoniaco anhidro (amoniaco puro en estado líquido bajo presión) se inyecta directamente en el suelo en algunas prácticas agrícolas, especialmente en grandes extensiones, como una fuente concentrada de nitrógeno.
¿De dónde se obtiene la materia prima principal del amoniaco?
Las materias primas principales son el nitrógeno del aire y el hidrógeno, que actualmente se obtiene mayoritariamente del gas natural (para amoniaco gris) o del agua mediante electrólisis con energía renovable (para amoniaco verde). El carbón también es una fuente importante de hidrógeno en algunas regiones.
Conclusión
El amoniaco es un compuesto químico de una importancia capital para la humanidad, principalmente debido a su papel insustituible en la producción de alimentos a través de los fertilizantes. El proceso de Haber-Bosch, junto con décadas de innovaciones tecnológicas en diseño de plantas, catalizadores y optimización energética, ha permitido que su producción industrial alcance las vastas escalas necesarias para satisfacer la demanda global.
Mirando hacia el futuro, la industria del amoniaco se enfrenta al desafío de reducir su impacto ambiental. La transición hacia el amoniaco verde, utilizando hidrógeno producido a partir de fuentes renovables, representa un paso crucial para descarbonizar la producción agrícola y abrir nuevas posibilidades para el amoniaco como vector energético. La historia de la producción de amoniaco es un testimonio del ingenio humano y su capacidad para transformar elementos simples en compuestos de valor incalculable para el progreso social y económico.
Si quieres conocer otros artículos parecidos a Obtención Industrial del Amoniaco (NH3) puedes visitar la categoría Industria.